Die tumortherapie-induzierte Diarrhoe (TID) tritt je nach Regime bei einem Großteil der behandelten Patient:innen auf. Besonders hohe Raten finden sich bei Fluoropyrimidinen (5-FU, Capecitabin) und Irinotecan sowie bei Kombinationsregimen wie FOLFIRI oder FOLFOXIRI. Auch zielgerichtete Substanzen verursachen in relevantem Ausmaß Diarrhoe: Bestimmte Tyrosinkinase-Inhibitoren zeigen in klinischen Studien Grad-3/4-Inzidenzen von teils über 10–20 %.
Schwere Verläufe gehen mit erheblicher Morbidität einher – Dehydratation, Elektrolytstörungen, Niereninsuffizienz und Sepsis sind mögliche Konsequenzen. Therapiepausen, Dosisreduktionen und Hospitalisierungen gefährden zusätzlich den Erfolg der Tumortherapie.
Was im Darm passiert – und warum es substanzspezifisch ist
Klassische Zytostatika schädigen die Epithelzellen des Gastrointestinaltrakts direkt und verursachen eine intestinale Mukositis mit Zottenatrophie, erhöhter Permeabilität und sekretorischer Dysfunktion. Irinotecan nimmt eine Sonderstellung ein: Es verursacht ein frühes cholinerges Syndrom (innerhalb von 24 h, durch Acetylcholinesterase-Hemmung) sowie eine verzögerte Mukosaschädigung durch den aktiven Metaboliten SN-38 (> 24 h) – beide Formen erfordern ein jeweils eigenes therapeutisches Vorgehen. Bei zielgerichteten Substanzen ist die Pathogenese bislang weniger gut verstanden.
Genetisches Risiko erkennen – Pharmakogenetik als Beratungsaufgabe
Zwei genetische Besonderheiten sind besonders praxisrelevant: Ein Mangel an Dihydropyrimidin-Dehydrogenase (DPD) durch DPYD-Varianten (DPYD2A, DPYD13, c.2846A>T, HaplotypB3) erhöht das Toxizitätsrisiko unter Fluoropyrimidinen erheblich. Die S3-Leitlinie empfiehlt die Testung auf diese vier Varianten vor Therapiebeginn mit 5-FU, Capecitabin oder Tegafur mit dem höchsten Empfehlungsgrad (Grad A, Evidenzlevel 1) – eine EMA-Empfehlung, die seit 2020 in den Fachinformationen verankert ist. Bei Irinotecan kann ein UGT1A1*28-Polymorphismus den Abbau des Metaboliten SN-38 verlangsamen und u. a. das Diarrhoerisiko erhöhen; eine Routinetestung wird nicht empfohlen, ist aber nach schwerer Toxizität zu erwägen. Pharmazeut:innen können hier prüfen, ob eine DPYD-Testung dokumentiert ist.
Wer ist besonders gefährdet?
Zu den allgemeinen Risikofaktoren zählen höheres Lebensalter, reduzierter Allgemeinzustand, simultane Radiotherapie im Bauch-Becken-Bereich, vorbestehende Darmdysfunktionen (z. B. Reizdarmsyndrom, Zöliakie, Gallensäuremalabsorption), vorangegangene Darmoperationen, Stoma sowie Mangelernährung. Differenzialdiagnostisch muss vor allem eine infektiöse Genese ausgeschlossen werden – allen voran Clostridioides difficile, besonders bei vorausgegangener Antibiotikagabe oder Hospitalisierung. Weitere Ursachen umfassen Strahlenenteritis, andere medikamentös bedingte Diarrhoe sowie neu aufgetretene Intoleranzen. Nicht jede Diarrhoe unter Tumortherapie ist eine TID.
Schweregrad einschätzen und richtig handeln
Die Einteilung nach den Common Terminology Criteria for Adverse Events (CTCAE, Version 5.0) ist das etablierte Instrument zur Schweregraderfassung:
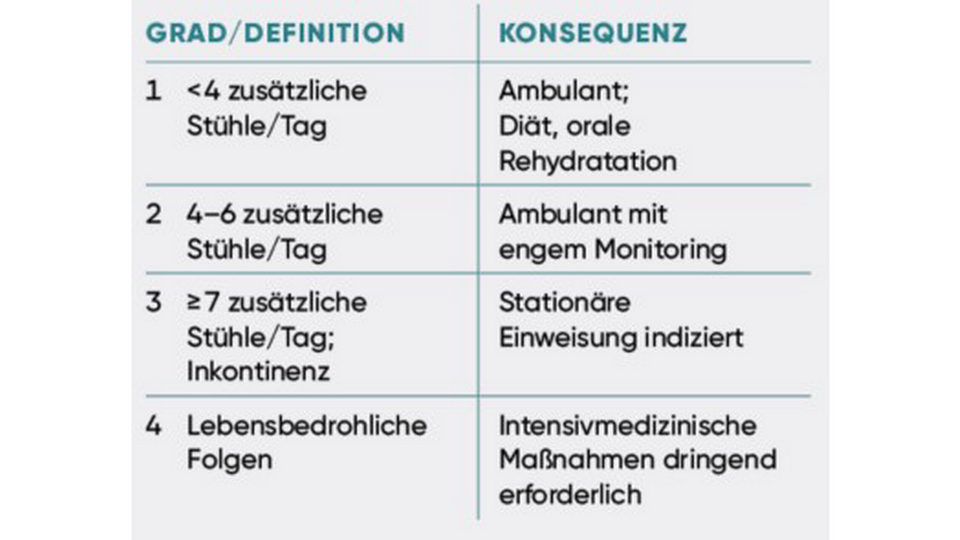
Klinisch entscheidende Parameter wie Fieber, Neutropenie, Krämpfe und Hypovolämie sind im CTCAE meist nicht abgebildet, müssen aber ergänzend erfasst werden – sie können auch bei Grad 1–2 eine sofortige Einweisung notwendig machen.
Bei unkomplizierter TID stehen Ernährungsanpassung, orale Rehydratation und Loperamid als Erstlinientherapie im Vordergrund. Da die Dosierung hier die Fachinformation überschreitet, müssen Patient:innen explizit darüber aufgeklärt werden; zudem ist auf das Risiko kardialer Ereignisse bei Überdosierung hinzuweisen.
Bei Loperamid-Refraktärität oder komplizierter Diarrhoe ist stationäre Einweisung indiziert.
Red Flags
Blut im Stuhl
Fieber
Starke Bauchschmerzen oder Krämpfe
Übelkeit und Erbrechen, die Trinken unmöglich machen
Zeichen der Dehydratation (Schwindel, verminderte Harnmenge, trockene Schleimhäute)
Bekannte oder vermutete Neutropenie
Diarrhoe Grad 3 oder 4 (≥ 7 zusätzliche Stühle/Tag)
Keine Besserung auf Loperamid innerhalb von 12–24 Stunden
Schwerwiegende Verschlechterung des Allgemeinzustandes
Als Zweitlinienoptionen nennen beide Leitlinien Octreotid s. c. (OFF-LABEL), Tinctura opii, Budesonid sowie Racecadotril. Beim akuten cholinergen Syndrom unter Irinotecan soll Atropinsulfat verabreicht werden. Eine medikamentöse Prophylaxe ist aktuell für kein Tumortherapieregime als Standard belegt.
Die Apotheke als erste Anlaufstelle
Triaging
Das strukturierte Erfragen von Stuhlfrequenz, Blutbeimengungen, Fieber, Hydratationsstatus und Allgemeinzustand ist die wichtigste Aufgabe im Erstkontakt. Die Checkliste oben unterstützt dabei.
OTC-Beratung
Neben Loperamid stehen weitere Substanzen zur Verfügung – stets in Abstimmung mit dem Behandlungsteam und mit dem Hinweis auf die im onkologischen Kontext limitierte Evidenz. Racecadotril hemmt die intestinale Sekretion ohne Motilitätshemmung und ist bei Kontraindikationen gegen Loperamid eine sinnvolle Alternative; die ESMO-Leitlinie empfiehlt es bei Immuntherapie-induzierter Diarrhoe.
Barriereprotektive Substanzen wie Hydroxypropylmethylcellulose mit Gellan Gum sowie Gelatinetannat sind pathophysiologisch plausibel, bisher liegen nur begrenzt onkologische Hinweise vor. Calciumaluminosilicat zeigte in einer randomisierten Studie keinen signifikanten Vorteil und wird nicht zur Prophylaxe empfohlen. Zinkacetat kann die Epithelregeneration unterstützen; spezifische onkologische Daten fehlen.
Ernährungsberatung
Die Leitlinien empfehlen die Vermeidung von Laktose, Alkohol, Koffein und Gewürzen sowie die Reduktion unlöslicher Ballaststoffe.
Interaktionsprüfung
Loperamid ist Substrat von P-Glykoprotein und CYP3A4; relevante Interaktionen bestehen mit Azol-Antimykotika, Makrolid-Antibiotika und Cimetidin. Bei Capecitabin ist das CYP2C9-Interaktionspotenzial (v. a. mit Warfarin) zu prüfen.
Blick nach vorn
Das intestinale Mikrobiom als Mediator der TID rückt zunehmend in den Forschungsfokus. Veränderungen in Diversität und Zusammensetzung unter Fluoropyrimidinen wurden beschrieben. Probiotika und fäkaler Mikrobiomtransfer werden als präventive Strategien erforscht; Leitlinien sehen die Datenlage jedoch als unzureichend für eine Routineempfehlung. Bis belastbare Daten vorliegen, bleibt das leitlinienkonforme Stufenmanagement der Goldstandard – und die Apotheke ein unverzichtbarer Baustein in der Versorgungskette.
Quellen
1 S3-Leitlinie: Supportive Therapie bei onkologischen PatientInnen (2025) Kapitel 6: Tumortherapie-induzierte Diarrhoe. AWMF Reg.Nr. 032/054OL
2 Bossi P, et al. Diarrhoea in adult cancer patients: ESMO Clinical Practice Guidelines. Ann Oncol 2018;29(Suppl 4):iv126–iv142. https://doi.org/10.1093/annonc/mdy145
3 Kawasaki Y et al. Relationship between chemotherapy-induced diarrhea and intestinal microbiome. Digestion. 2023;104(5):357–366. https://doi.org/10.1159/000528282