ie chronische Herzinsuffizienz (HI) stellt mit schätzungsweise 250.000 bis 300.000 Betroffenen eine der größten medizinischen Herausforderungen in Österreich dar. Rund jede/r zehnte hospitalisierte Patient:in wird mit der Hauptdiagnose „Herzinsuffizienz“ entlassen. Nach Diagnosestellung liegt die 5-Jahres-Überlebensrate statistisch bei ca. 50 %. Erfreulicherweise haben moderne Therapien die Lebenserwartung und Lebensqualität zuletzt deutlich verbessert.
HFrEF versus HFpEF
Chronische HI ist ein Syndrom, das sich klinisch durch Belastungsdyspnoe, Müdigkeit und Flüssigkeitsretention (periphere Ödeme, rasche Gewichtszunahme) auszeichnet und anhand objektivierbarer Parameter einer kardialen Dysfunktion diagnostiziert wird (v. a. Echokardiographie, Biomarker NT-proBNP-Wert > 125 pg/ml). Ursächlich ist eine strukturelle und/oder funktionelle Herzerkrankung mit erhöhten intrakardialen Füllungsdrücken und/oder inadäquatem Herzzeitvolumen.
Die Klassifikation erfolgt primär anhand der Symptomstärke (NYHA-Klassen I–IV) und echokardiographischen Pumpfunktion. Eine HI mit reduzierter linksventrikulärer Ejektionsfraktion (HFrEF) liegt bei einer LVEF ≤ 40 % vor und ist durch eine systolische Pumpfunktionsstörung mit starker neurohumoraler Aktivierung charakterisiert. HFrEF entspricht dem klassischen Bild einer chronischen HI.
Demgegenüber wird die HI mit erhaltener Ejektionsfraktion (HFpEF) durch eine LVEF von ≥ 50 % definiert. Grundlegende Merkmale dieser HI-Form sind diastolische Dysfunktion, Gefäßendothelschädigung und systemische Inflammation. Vereinfacht ausgedrückt ist die Pumpfunktion bei HFpEF noch erhalten, das Myokard aber schon „steif“, was sich in einer heterogenen Klinik widerspiegelt, die häufig mit Adipositas, Diabetes, Hypertonie und chronischer Niereninsuffizienz assoziiert ist. HI mit mäßig eingeschränkter LVEF (HFmEF; LVEF 41–49 %) nimmt gewissermaßen eine Zwischenstellung ein. Die European Society of Cardiology (ESC) weist außerdem auf den neuen Begriff HFimpEF hin (HI mit verbesserter Ejektionsfraktion), für Patient:innen, die zuvor eine HFrEF hatten und nun infolge einer Therapie eine LVEF von > 40 % aufweisen.
Medikamentöse Behandlung der HFrEF
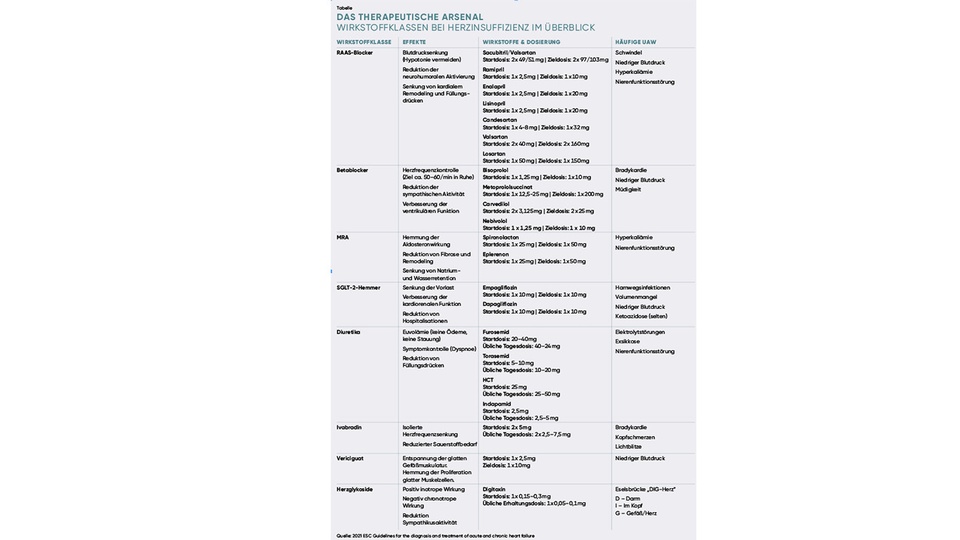
Die pharmakologische Therapie der HFrEF zielt darauf ab, die neurohumorale Aktivierung zu modulieren. Sie basiert auf einer Kombination mehrerer prognoseverbessernder Substanzklassen, die frühzeitig initiiert und auf die entsprechende Zieldosis titriert werden sollten (siehe Tabelle, Seite 42).
RAAS-Blocker
Grundlage bildet die Hemmung des Renin-Angiotensin-Aldosteron-Systems (RAAS), wobei entweder ACE-Hemmer bzw. Angiotensin-Rezeptorantagonisten oder Angiotensin-Rezeptor-Neprilysin-
Inhibitoren (ARNI) eingesetzt werden. ARNI er-
wiesen sich gegenüber ACE-Hemmern prognostisch als überlegen, insbesondere hinsichtlich Mortalität und Hospitalisierungsrate. Sie werden deshalb zu-
nehmend als First-Line-Therapie empfohlen.
Betablocker
Was sich zur Jahrtausendwende kaum einer vorstellen konnte, ist heute Standard. Nachdem retardiertes Metoprolol und Carvedilol in MERIT-HF und COPERNICUS die Mortalität bei chronischer HI senken konnten, gelang der Nachweis später auch für Bisoprolol und Nebivolol. Mittlerweile fungieren diese vier Betablocker als zentrale Säule der medikamentösen Behandlung der chronischen HI, da sie die sympathische Überaktivität verringern und LVEF verbessern.
MRA
Mineralokortikoid-Rezeptorantagonisten (MRA) wie Spironolacton oder Eplerenon ergänzen die neurohumorale Blockade, indem sie die Wirkung von Aldosteron hemmen. Sie führen nachweislich zu einer signifikanten Reduktion von Mortalität und Hospitalisationen. Darüber hinaus verringern ihre antifibrotischen Eigenschaften das unerwünschte ventrikuläre Remodeling.
SGLT-2-Inhibitoren
Dapagliflozin und Empagliflozin sind die letzte wesentliche Erweiterung der HI-Therapie. In EMPEROR-Reduced und DAPA-HF reduzierten sie un-
abhängig vom Vorliegen eines Diabetes Mortalität und Hospitalisierungsrate aufgrund von HI. Die zugrunde liegenden Mechanismen sind multifaktoriell. Beschrieben sind ein verbesserter Energiestoffwechsel sowie natriuretische und antiinflammatorische Effekte. Ihr Einsatz wird gegenwärtig auch bei akuter HI diskutiert.
Diuretika
Diuretika werden bei chronischer HI gegen Stauungsödeme zur Volumenentlastung und Symptomkontrolle eingesetzt. Die Indikation sollte regelmäßig reevaluiert werden.
Andere Substanzen
Bei persistierenden Symptomen oder speziellen Konstellationen sind zusätzliche Substanzen verfügbar. Darunter Ivabradin, zur Frequenzkontrolle bei Sinusrhythmus, und Vericiguat, zur Modulation des NO-sGC-cGMP-Signalwegs bei Patient:innen mit fortgeschrittener Herzinsuffizienz, die nach einem kürzlich aufgetretenen Dekompensationsereignis, das eine i.v.-Therapie erforderte, stabilisiert wurden. Früher großzügig verordnete Herzglykoside haben in der modernen HI- und Rhythmustherapie nur noch sehr spezifische Anwendungsgebiete. Dazu zählen die symptomatische HFrEF trotz optimaler Standardtherapie oder Patient:innen mit Vorhofflimmern, die nicht auf Betablocker oder Kalziumantagonisten ansprechen oder diese nicht vertragen.
HFrEF:
Was hat sich geändert?
Die ESC-Leitlinien von 2021 führten die sogenannte „Vier-Säulen-Therapie“, bestehend aus ARNI/ACE-Hemmer, Betablocker, MRA und SGLT-2-Inhibitoren, als Standard der HFrEF-Behandlung ein. Die vier Substanzklassen werden als gleichwertig essenziell betrachtet und sollten allen geeigneten Patient:innen verschrieben werden. Das 2023-Update entwickelte diesen Ansatz weiter.
Der Fokus liegt nun klar auf einer frühzeitigen, simultanen Initiierung aller vier prognoseverbessernden Therapien anstelle eines sequenziellen Vorgehens. Ziel ist es, innerhalb weniger Wochen eine vollständige Basistherapie zu etablieren. Diese Strategie wird durch Studien wie STRONG-HF unterstützt, in denen gezeigt werden konnte, dass eine rasche Aufdosierung unter engmaschiger Kontrolle Rehospitalisierungen und Mortalität reduziert.
Weitere Neuerungen betreffen die stärkere Integration von Komorbiditäten in das Behandlungskonzept, etwa die Therapie des Eisenmangels mittels intravenöser Eisensubstitution.
Medikamentöse Behandlung der HFpEF/HFmEF
Für die pharmakologische Therapie der HFpEF/HFmEF gab es lange keine aussagekräftigen Endpunktstudien, um allgemeine Empfehlungen auszusprechen. Umso wichtiger waren Symptomkontrolle und die Behandlung etwaiger Komorbiditäten. Dafür verwendete Medikamente entsprechen denjenigen der HFrEF, sprich: RAAS-Blocker, Betablocker und MRA zur Behandlung begleitender Erkrankungen wie Hypertonie, koronarer Herzkrankheit oder Vorhofflimmern, allerdings ohne konsistenten Nachweis eines prognostischen Nutzens. Studien wie TOPCAT für Spironolacton oder PARAGON-HF für Sacubitril/Valsartan verliefen enttäuschend und zeigten nur begrenzte oder populationsabhängige Effekte.
HFpEF/HFmEF:
Was hat sich geändert?
Die ESC-Leitlinien von 2021 reflektieren die therapeutische Limitation, da keine medikamentöse Therapie mit eindeutigem prognostischen Benefit empfohlen werden konnte. Die entscheidende Wende kam schließlich im Update 2023, in dem mit den SGLT-2-Inhibitoren erstmals Medikamente eine Klasse-I-Empfehlung mit hohem Evidenzgrad für Patient:innen mit HFpEF und HFmrEF erhielten. Basis dieser Empfehlungen bilden die großen randomisierten Studien EMPEROR-Preserved und DELIVER. In EMPEROR-Preserved führte die tägliche Gabe von Empagliflozin bei Patient:innen mit HI und LVEF > 40 % zu einer signifikanten Reduktion des kombinierten Endpunkts aus kardiovaskulärem Tod und Hospitalisation wegen HI. DELIVER bestätigt diese Ergebnisse für Dapagliflozin, das über das gesamte Spektrum der LVEF hinweg konsistente Effekte zeigt, einschließlich Patient:innen mit zuvor reduzierter und später verbesserter EF (= HFimpEF). Wie schon bei HFrEF war die beobachtete Wirkung auf das Herz unabhängig vom Diabetesstatus. SGLT-2-Inhibitoren sind somit aktuell die einzige Substanzklasse, für die bei HFpEF/HFmEF ein reproduzierbarer prognostischer Benefit belegt ist.
Fazit
Die jüngsten ESC-Leitlinien verschieben den Fokus von der reinen Substanzwahl hin zu einer frühzeitigen und konsequenten Implementierung der HI-Therapie über das gesamte Spektrum der Ejektionsfraktion hinweg. Während für die HFrEF eine etablierte, evidenzbasierte Vierfachtherapie existiert, wurde für die HFpEF/HFmEF erst durch die Integration der SGLT-2-Inhibitoren eine Therapie mit gesichertem prognostischem Nutzen definiert.
Quellen
• McDonagh TA, et al.: 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2021;42(36):3599-3726
• McDonagh TA, et al.: 2023 Focused Update of the 2021 ESC Guidelines for the diagnosis and treatment of acute and chronic heart failure. Eur Heart J 2023 Oct 1;44(37):3627-3639