Die funktionelle Dyspepsie (FD; Reizmagen) ist eine der häufigsten gastroenterologischen Erkrankungen. Bis zu 10 % der Bevölkerung kämpfen im Laufe ihres Lebens mit dyspeptischen Symptomen und erfüllen damit zumindest vorübergehend die ROM-IV-Kriterien für eine nicht abgeklärte FD. Gemeinsam mit dem Reizdarmsyndrom gehört das Krankheitsbild zu den sogenannten Darm-Hirn-Interaktionsstörungen (Disorders of Gut-Brain Interaction; DGBI) – einer Gruppe von Erkrankungen, die man ehemals unter dem Terminus „funktionelle gastrointestinale Störungen (FGID)“ zusammenfasste und die bei betroffenen Patient:innen einen hohen Leidensdruck verursachen. Der Wechsel von FGID auf DGBI soll die tragende Rolle der Darm-Hirn-Achse bei der Entstehung und Aufrechterhaltung dieser funktionellen Erkrankungen des Verdauungstrakts betonen und den Weg für neue Behandlungsmethoden ebnen.
Definition und Pathophysiologie
FD bezeichnet wiederkehrende bzw. chronische Beschwerden des oberen Abdomens, die mit den verfügbaren diagnostischen Standardverfahren keiner organischen Ursache zugeordnet werden können. Demzufolge handelt es sich bei FD um eine Ausschlussdiagnose, deren Behandlungsziel die symptomatische Besserung der von Patient:innen berichteten Beschwerden ist. Für die Entstehung wurden verschiedene Risikofaktoren identifiziert, deren Einfluss auf die pathophysiologischen Prozesse bis dato nur teilweise im Detail verstanden ist.
Diesen Umstand adressiert auch die 2025 aktualisierte deutsche S1-Leitlinie „Reizmagen“. Demnach sind die zugrundeliegenden Mechanismen multifaktoriell bedingt und über das Modell der Darm-Hirn-Achse zu verstehen. Dazu zählen eine gestörte Magen- und Duodenalmotorik (verzögerte Magenentleerung, reduzierte antrale Kontraktion, postprandiale Dysmotilität), viszerale Hypersensitivität (verstärkte Wahrnehmung von Dehnung oder chemischen Reizen im oberen Gastrointestinaltrakt), erhöhte Schleimhautdurchlässigkeit, subtile inflammatorische Prozesse sowie veränderte enterische und zentrale neuronale Signalwege. Psychosoziale Faktoren wie Stress, Angst oder frühkindliche Traumata werden als Modulatoren der Symptom-Entwicklung und -Aufrechterhaltung betrachtet.
So präsentiert sich FD
Infolgedessen verstehen Fachgesellschaften FD als einen Symptomkomplex, in dessen Verlauf die beschriebenen Mechanismen interagieren und sich beschwerdearme/-freie Intervalle mit beschwerdereichen abwechseln können. Leitsymptome sind ein frühes Sättigungsgefühl, postprandiales Völlegefühl, epigastrische Schmerzen und epigastrisches Brennen. Blähungen, Übelkeit, Sodbrennen und Aufstoßen werden den Begleitsymptomen zugeordnet. Das variable Erscheinungsbild trägt zur verzögerten Diagnosestellung bei.
Die Rome Foundation überarbeitet derzeit ihre Richtlinien für die Diagnose und Behandlung von „Disorders of Gut-Brain Interaction“ (DGBI) – also Erkrankungen, bei denen Darm und Gehirn zusammenspielen. Die neuen Rom-V-Kriterien sollen 2026 fertiggestellt werden und werden erstmals Themen wie Mikrobiom, Ernährung, Geschlechts- und Altersunterschiede, Zusammenhänge mit anderen Erkrankungen sowie kulturelle Unterschiede umfassend berücksichtigen.
FD richtig diagnostizieren
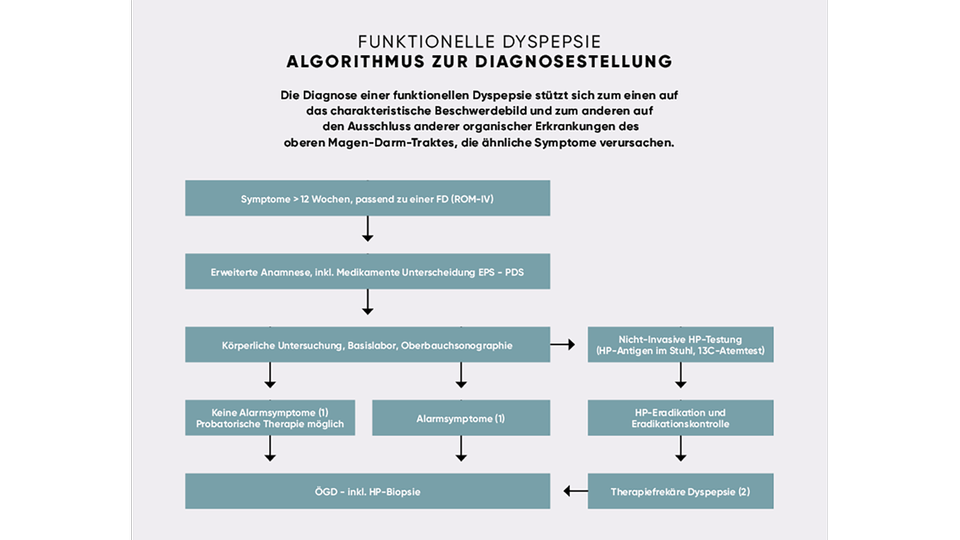
Von ärztlicher Seite wird überprüft, ob typische Symptome vorhanden und strukturelle bzw. organische Ursachen plausibel sind. Beim Vorliegen von Alarmsymptomen ist eine weiterführende Diagnostik erforderlich. Für die Praxis empfiehlt die S1-Leitlinie bei zu FD passenden Beschwerden eine Basisuntersuchung mit Blutbild, Entzündungsparametern, Leberwerten, Sonografie des Oberbauchs sowie nicht-invasiver Testung auf Helicobacter pylori (z. B. Atemtest, Stuhltest) mit anschließender Eradikation bei Nachweis. Letzteres ist klinisch besonders relevant, da H. pylori bei einer Untergruppe von Patient:innen maßgeblich an der Entstehung und Aufrechterhaltung der Beschwerden beteiligt ist.
Eine Ösophagogastroduodenoskopie ist insbesondere beim Vorliegen von Alarmsymptomen, beim erstmaligen Auftreten im höheren Lebensalter (> 50 Jahren) oder bei unklaren Befunden indiziert. Von einer therapierefraktären Dyspepsie spricht man dann, wenn bei H. pylori-positiven Patient:innen die Symptome 6–12 Monate nach bestätigter Eradikation weiter fortbestehen. Bei Patient:innen mit Dyspepsie und endoskopisch nachgewiesener H. pylori-negativer Gastritis wird von einer FD als Ursache der Beschwerden ausgegangen.
Medikamentöse Therapie
Mittel der Wahl bei therapierefraktärer Dyspepsie und FD sind niedrigdosierte Protonenpumpeninhibitoren (PPI; off-label bei säurebedingten Symptomen) und Phytotherapeutika wie STW-5 (Iberis Amara, Pfefferminze, Kamille, Kümmel, Melisse, Süßholz, Angelikawurzel, Mariendistel, Schöllkraut) und STW-5-II (Iberis Amara, Kamille, Kümmel, Melisse, Pfefferminze, Süßholz). Patient:innen mit starkem Gewichtsverlust sollte eine Ernährungsunterstützung angeboten werden. Bei fehlender oder unzureichender Wirkung der Erstlinientherapie ist es therapeutisch sinnvoll, die FD weiter in das postprandiale Distress-Syndrom (PDS) bzw. das Epigastrische Schmerzsyndrom (EPS) zu unterteilen und einen mechanismenbasierten Ansatz zu verfolgen.
• Schluckstörung und/oder Schmerzen beim Schlucken
• Rezidivierendes oder persistierendes Erbrechen
• Ungewollter Gewichtsverlust
• Gastrointestinale Blutungszeichen
(z. B. Erbrechen von Blut, teerartiger Stuhl)
• Gelbsucht
• Fieber oder Nachtschweiß
• Erstsymptomatik im höheren Lebensalter
• Familiäre Belastung mit Magen- oder Kolonkarzinomen
Für das PDS, bei dem eine verringerte gastrointestinale Motilität und mahlzeitenbedingte Symptome im Vordergrund stehen, stellen Prokinetika einen vielversprechenden Ansatz dar, der eine Chance auf symptomatische Besserung bietet. Im Fall von Gewichtsverlust oder früher Sättigung sind 5-HT1A-Agonisten eine Option. Demgegenüber können Patient:innen mit EPS und den damit einhergehenden prädominant epigastrischen, mahlzeitenunabhängigen Oberbauchschmerzen von niedrigdosierten trizyklischen Antidepressiva profitieren. Positive klinische Studien in der medikamentösen Zweitlinientherapie existieren für Amitriptylin, Mirtazapin und Sulpirid. Patient:innen sollten über das Nebenwirkungsprofil aufgeklärt werden.
Rolle von Nahrungsmitteln bei FD
Obgleich der Einfluss von Nahrung auf die FD nachvollziehbar erscheint, gibt es keine hinreichende Evidenz für ernährungsspezifische Empfehlungen. Duncanson et al. (2018) konnten in einer umfangreichen systematischen Analyse von 16 Studien keinen konsistenten Zusammenhang zwischen FD-Symptomen und Nahrungsaufnahme feststellen. In einer rezenteren Arbeit (Colomier et al. 2022) gaben von über 54.000 Befragten immerhin 11 % an, regelmäßig unter nahrungsmittelassoziierten Beschwerden im oberen und unteren Gastrointestinaltrakt zu leiden, auch wenn diese nicht zwingend mit einer FD in Verbindung standen. Randomisiert kontrollierte Studien zu diätetischen Interventionen bei Patient:innen mit FD gibt es bisher keine. Auch die low-FODMAP-Diät kann bei der FD nicht empfohlen werden. Statt spezifischer Ernährungsempfehlungen sollten allgemeine Hinweise gegeben werden: kleine, verträgliche Mahlzeiten, ausreichende Flüssigkeitszufuhr und das Vermeiden großer oder hastiger Nahrungsaufnahmen. Eine individuelle Ernährungsberatung kann unterstützen, Diäten nur bei klarer Symptomverbesserung fortführen.
Take-Home-Message
Funktionelle Dyspepsie ist eine der häufigsten gastroenterologischen Erkrankungen, die aufgrund variabler Symptomatik und zahlreicher Differenzialdiagnosen viel Zeit und Patientenzuwendung erfordert. Viele All-
gemeinmediziner:innen stehen vor dem Problem, dass eine konsequente Betreuung der gesprächsintensiven FD-Patient:innen oft nicht oder nur schwer umsetzbar ist. Hier können Apotheker:innen eine unterstützende Rolle übernehmen und allgemeinmedizinische Praxen durch Erfragen von Alarmsymptomen und ggf. Verweis an den Arzt bzw. die Ärztin sowie niederschwellige Folgekontakte entlasten.
Eine nichtinvasive H. pylori-Diagnostik mit etwaiger Eradikation ist generell bei allen Patient:innen empfohlen, die über länger anhaltende dyspeptische Beschwerden berichten. Für nach wie vor symptomatische und H. pylori-negative Patient:innen mit persistierenden Beschwerden trotz Eradikation bietet sich ein Therapieversuch mit niedrigdosierten PPI und/oder Phytopharmaka an. Bei fehlendem oder unzureichendem Effekt ist eine Unterscheidung zwischen PDS und EPS nötig, da dies die Wahl der Zweitlinientherapie beeinflusst.
QuelleN
• Colomier E, et al.: Global prevalence and burden of meal-related abdominal pain. BMC Med 2022; 20(1):71
• Drossman, DA: Functional Gastrointestinal Disorders: History, Pathophysiology, Clinical Features and Rome IV. Gastroenterology. 2016; S0016-5085(16)00223-7.
• Duncanson, KR et al.: Food and functional dyspepsia: a systematic review. J Hum Nutr Diet 2018; 31(3):390-407
• Sperber AD, et al.: Worldwide prevalence and burden of functional gastrointestinal disorders, results of Rome Foundation Global Study. Gastroenterology 2021; 160(1):99-114.e3
• Stanghellini V, et al.: Gastroduodenal Disorders. Gastroenterology 2016; 150(6):1380-92
Weitere Literatur auf Anfrage