Eine chronische Nierenerkrankung (CKD) betrifft in Österreich ungefähr 10 % der Bevölkerung, also 800.000–970.000 Menschen.2 Definiert wird sie durch die internationale Fachorganisation KDIGO (Kidney Disease Improving Global Outcomes) folgendermaßen: „Eine chronische Nierenerkrankung ist eine über mindestens drei Monate bestehende Veränderung der Nierenstruktur oder -funktion, die gesundheitliche Auswirkungen hat.“3 Die Prävalenz bei Frauen ist etwas höher als bei Männern. Neben der altersbedingten, physiologischen Abnahme der glomerulären Filtrationsrate tragen vor allem verschiedene Begleiterkrankungen zu einer Verschlechterung der Nierenfunktion bei. Zu den wichtigsten Risikofaktoren zählen Diabetes mellitus und arterielle Hypertonie, die zusammen etwa 45 % aller Nephropathien verursachen. Menschen mit Typ-2-Diabetes haben eine 20–50%ige Wahrscheinlichkeit, im Laufe ihres Lebens eine chronische Nierenerkrankung zu entwickeln. Bluthochdruck kann zum einen die Ursache einer CKD sein, aber auch die Folge davon.4
Folgen der chronischen Nierenerkrankung
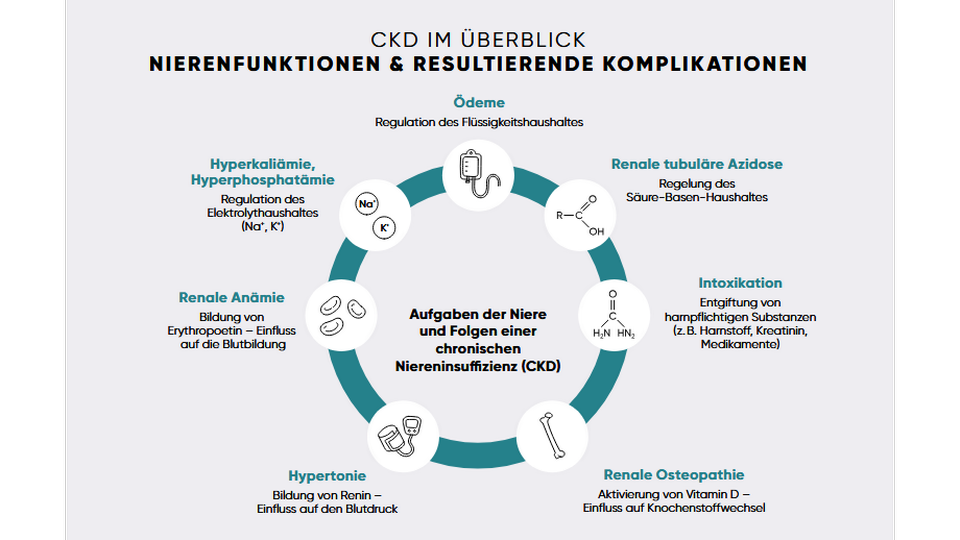
Die Folgen einer chronischen Niereninsuffizienz sind so vielfältig wie auch die Aufgaben, die die Niere im Körper übernimmt.
Klassifikation und Einteilung der CKD
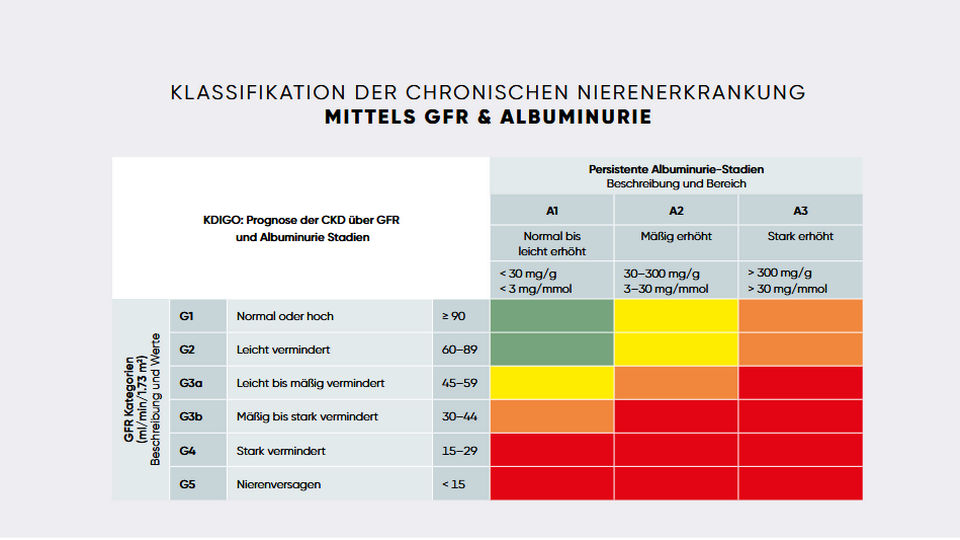
Die Klassifikation der chronischen Nierenerkrankung erfolgt nach der Ursache der CKD (Cause), der Kategorie der glomerulären Filtrationsrate (GFR, G1–G5) sowie nach Albuminurie (A1–A3) und wird mit „CGA“ abgekürzt. Die Bestimmung des Schweregrades findet international nach der Einteilung der KDIGO statt, die eGFR- und Albuminurie-Stadien (Albumin-Kreatinin-Ratio) zusammenfasst.3 Die Ernährungstherapie bei chronisch Nierenerkrankten muss die verschiedenen metabolischen Veränderungen in den einzelnen Stadien der Nierenfunktionseinschränkung berücksichtigen. Ein zentraler Punkt dabei ist die Differenzierung, ob der/die Patient:in bereits ein Nierenersatzverfahren in Anspruch nimmt oder nicht (Hämodialyse oder Peritonealdialyse).
Prädialysephase
Das Therapieziel in den frühen Phasen der Niereninsuffizienz ist das Hinauszögern einer Progression der Funktionseinschränkung. Epidemiologische Daten zeigen, dass eine kaliumreiche, kochsalzarme und pflanzenbasierte Ernährung, wie sie z. B. in der mediterranen Ernährung oder in der DASH-Diät vorkommt, mit einem niedrigen Risiko für eine CKD behaftet ist. Diese Ernährungsform wird auch bei kardiovaskulären Erkrankungen und Diabetes empfohlen. Aber auch bei einer bereits bestehenden CKD Stadium G3a–G5 ist eine Ernährung mit hohem pflanzlichen Proteinanteil von Vorteil im Hinblick auf die Sterblichkeitsrate.4

Hohe Proteinanteile galten bei der Niereninsuffizienz immer als zweischneidiges Schwert: Es können sich Proteinabbauprodukte wie Harnstoff, p-Cresylsulfat oder Indoxylsulfat im Blut anreichern (Urämietoxine). Eine eiweißarme Ernährung kann deren Bildung und die Hyperfiltration verringern und wirkt potenziell nephroprotektiv. Noch vor 30 Jahren galt die Empfehlung einer sehr strengen eiweißarmen Kost (< 0,6 g/kg KG/Tag). Neuere Daten und Metaanalysen haben jedoch gezeigt, dass die strenge eiweißarme Diät keinen Effekt auf die Mortalität und das Voranschreiten der terminalen Niereninsuffizienz hatte. Darüber hinaus war die Gefahr, eine Mangelernährung zu entwickeln, deutlich höher und zudem problematischer. In nur mehr sehr seltenen Fällen wird eine starke eiweißarme Kost empfohlen. Die momentane Empfehlung liegt bei einer moderaten Senkung der Proteinzufuhr auf 0,6–0,8 g/kg/Tag und stellt damit die eigentliche Empfehlung der Deutschen Gesellschaft für Ernährung (DGE) für gesunde Menschen dar. Proteinlieferanten sollten dabei zur Hälfte pflanzliche Proteine sein und zur anderen Hälfte Proteine mit einer hohen biologischen Wertigkeit, wie beispielsweise die Kombinationen von Kartoffeln und Eiern. Eine Zufuhr von über 1,3 g/kg/Tag sollte vermieden werden.4,5
Die Trinkmenge sollte bedarfsdeckend laut normaler DGE-Empfehlungen bei 20–30 ml/kg KG/Tag liegen. In den Stadien 1–5 der CKD tritt, außer bei Patient:innen mit komorbider Herzschwäche, kein Rückgang der Urinmenge auf. Je nach äußeren Umständen (Fieber, Hitze) oder Begleiterkrankungen (Herzinsuffizienz) sollte die Trinkmenge angepasst werden. Patient:innen sollten auf Überwässerungen und folglich auf Einlagerungen von Flüssigkeit (Ödeme) achten. Therapierefraktäre Überwässerungen stellen dabei eine Indikation für eine Dialysepflicht dar.4,5
Im Hinblick auf die Kochsalzzufuhr gelten für Patient:innen mit chronischer Nierenerkrankung ähnliche Empfehlungen wie für die Allgemeinbevölkerung: Die Kochsalzzufuhr sollte 5–6 g/Tag nicht überschreiten. Kaliumrestriktionen (< 4.000 mg/Tag) sind nur im Prädialysestadium bei nachgewiesener Hyperkaliämie erforderlich. Eine therapierefraktäre Hyperkaliämie ist zwar eine absolute Dialyseindikation, tritt jedoch meist erst im Endstadium auf. Dagegen kann eine metabolische Azidose bereits früh (GFR < 40–50 ml/min) auftreten und sollte durch eine Blutgasanalyse überwacht werden.5
Therapeutisch kommt bei einem Bikarbonatspiegel < 22 mmol/l eine Behandlung mit Natriumhydrogencarbonat in Betracht. Zusätzlich wirkt sich eine obst- und gemüsereiche Ernährung positiv auf das Säure-Basen-Gleichgewicht aus, senkt die Hyperkaliämie und vermindert katabole Prozesse. So können Muskelmasse und -kraft besser erhalten und der Knochenstoffwechsel unterstützt werden.4,5
Eine Studie an CKD-G4-Patient:innen zeigte sogar, dass eine erhöhte Obst- und Gemüsezufuhr der reinen Bikarbonatsubstitution überlegen war, nicht nur in Bezug auf die CKD-Progression, sondern auch hinsichtlich Blutdruckkontrolle, Lipidprofil, Vitaminstatus und weiterer kardiovaskulärer Risikofaktoren. Für CKD-Stadien G1–4 wird daher eine obst- und gemüsereiche Ernährung empfohlen, um die endogene Säurelast zu senken und das Fortschreiten der Erkrankung zu verlangsamen.4
Bei nierengesunden Menschen treten Hyperphosphatämien nur selten auf. Da Phosphat jedoch überwiegend über die Nieren ausgeschieden wird, können dauerhaft erhöhte Serumspiegel die kardiovaskuläre Gesundheit beeinträchtigen und sind mit einer erhöhten Mortalität assoziiert. Für die Allgemeinbevölkerung wird eine tägliche Phosphatzufuhr von rund 700 mg empfohlen. Eine Reduktion der Aufnahme lässt sich über eine eiweißkontrollierte Ernährung erreichen. Dabei ist zu berücksichtigen, dass Phosphat aus pflanzlichen Lebensmitteln schlechter resorbiert wird als jenes aus tierischen Quellen wie Fleisch oder Milchprodukten. Besonders relevant ist zudem der hohe Phosphatgehalt in industriell verarbeiteten Lebensmitteln, die häufig mit Phosphatsalzen angereichert werden. Sei es für die Fähigkeit der Wasserbindung, Stabilisierung, Emulgierung oder als Säureregulator. Diese chemisch zugesetzten Phosphatverbindungen stellen aufgrund der sehr hohen Bioverfügbarkeit ein Problem dar.5,6
Dialysephase
In der Dialysephase stehen zwei zentrale Ziele der Ernährungstherapie im Vordergrund: die Vermeidung einer Mangelernährung sowie die Senkung des kardiovaskulären Risikos, das häufig durch Kaliumentgleisungen und Hyperphosphatämien verstärkt wird.
Da während der Dialyse Aminosäuren über das Dialysat verloren gehen, ist im Vergleich zur Prädialysephase eine eiweißreichere Ernährung erforderlich. Für Hämodialysepatient:innen wird eine Proteinzufuhr von > 1,1 g/kg Körpergewicht pro Tag empfohlen, bei Peritonealdialyse liegt der Richtwert bei 1,2–1,4 g/kg Körpergewicht.5
Da eine Hyperphosphatämie ein häufiges Problem darstellt, sollten phosphatarme Lebensmittel bevorzugt werden. Hierbei spielt der Phosphat-Eiweiß-Quotient (PEQ) eine wichtige Rolle, der idealerweise unter 14 mg/g liegen sollte. Besonders pflanzliche Phosphatquellen sind günstig, da hier weniger Phosphat vom Körper durch die Komplexierung mit den enthaltenen Phytinsäuren resorbiert wird.5
Die Kochsalzzufuhr sollte 5 g pro Tag nicht überschreiten. Dies trägt nicht nur zur Blutdruckkontrolle bei, sondern vermindert auch das Durstgefühl und reduziert Gewichtszunahmen zwischen den Dialysen, wodurch nachweislich die Sterblichkeit reduziert werden konnte.5 Die tägliche Trinkmenge richtet sich nach dem Dialyseintervall: Im langen Intervall (drei Tage zwischen zwei Hämodialysen) liegt die Empfehlung bei 500–800 ml/Tag, im kurzen Intervall bei bis zu 1,4 l. Ziel ist es, eine Überwässerung und die damit verbundenen Komplikationen wie Blutdruckbelastung oder Lungenödem zu vermeiden.5 Sowohl zu hohe als auch zu niedrige Kaliumwerte sind mit einer erhöhten Mortalität verknüpft.
Bei Hämodialysepatient:innen mit Hyperkaliämieneigung wird eine maximale Kaliumzufuhr von etwa 2.700 mg pro Tag empfohlen, da Blutwerte über 5,5 mmol/l das Sterblichkeitsrisiko deutlich erhöhen.5
Da wasserlösliche Vitamine während der Dialyse vermehrt verloren gehen und der Bedarf durch die Depletion des antioxidativen Systems sehr hoch ist, sollte einer Hypovitaminose vorgebeugt werden. In der Praxis wird die Zufuhr des doppelten Tagesbedarfs empfohlen (RDA = Recommended Dietary Allowance). Exakte Bedarfszahlen werden leider nicht genannt.1 L-Carnitin wird im menschlichen Körper aus den Aminosäuren L-Lysin und L-Methionin hergestellt und hat eine zentrale Rolle im Fettstoffwechsel. Mithilfe von L-Carnitin können beispielsweise Fettsäuren vom Cytosol in Zellorganellen wie den Mitochondrien transportiert werden.
Da bei der Dialyse L-Carnitin zu einem großen Teil verloren geht, kann eine Substitution von 0,5 g/Tag empfohlen werden. Dadurch sollen sich Symptome wie Müdigkeit und Schwäche, Muskelkrämpfe und Blutdruckschwankungen nach der Dialyse verbessern. Eine Cochrane-Analyse konnte keine gesicherte Evidenz dazu aufzeigen, merkt aber an, dass es sehr wohl Anämie-Marker (Hämoglobin und Hämatokrit) nachweislich verbessern konnte. Bei den anderen Anwendungsgebieten bräuchte es jedoch weitere Studien.1,7
Sowohl für Patient:innen als auch für Fachpersonal gibt es auf der Seite der Deutschen Gesellschaft für Nephrologie einen Ernährungsratgeber für Patient:innen, der sehr ausführlich die wichtigsten Ernährungsempfehlungen in den einzelnen Stadien der Niereninsuffizienz gibt.
Quellen
1 S1-Leitlinie : Enterale und parenterale Ernährung von Patienten mit Niereninsuffizienz (2015), AWMF Reg. Nr. 073/009
2 Alexander R. Rosenkranz & Michael Kolland: Chronische Niereninsuffizienz. Österr. Ärztezeitung 2023
3 Kidney Disease: Improving Global Outcomes (KDIGO) CKD work group: KDIGO 2024 Clinical practice guideline for the evaluation
and management of chronic kidney disease. Kidney Int 2024; 105(4S):S117-S314
4 S3-Leitlinie: Versorgung von Patient*innen mit chronischer, nicht-Nierenersatz-Therapiepflichtiger Nierenkrankheit (2024), AWMF Reg. Nr. 053 - 048
5 Rubin D, Winckler K: Praxishandbuch Ernährungsmedizin (2023), Elsevier
Weitere Literatur auf Anfrage