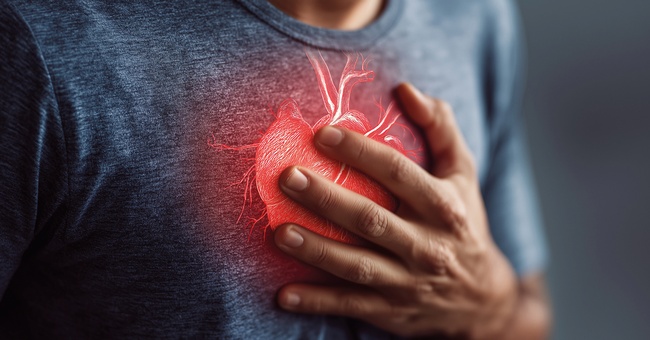
Tumortherapie-induzierte Übelkeit und Erbrechen, kurz CINV (chemotherapy-induced nausea and vomiting), zählen zu den am stärksten belastenden Nebenwirkungen onkologischer Therapien. Man unterscheidet eine akute von einer verzögerten Symptomatik. Die akute Emesis (welche innerhalb von 24 Stunden nach der Chemotherapie auftritt) wird überwiegend peripher getriggert: Zytostatika stimulieren enterochromaffine Zellen des Dünndarms zur Freisetzung von Serotonin, dieses bindet an die 5‑HT3‑Rezeptoren der benachbarten afferenten Vagusnerven und leitet stimulierende Impulse an den „Central Pattern Generator“, früher Brechzentrum genannt, in der Medulla oblongata weiter. Die verzögerte Emesis (welche nach 24 bis 120 Stunden, also zwischen dem ersten und dem fünften Tag nach der Behandlung auftritt) ist stärker zentral geprägt, primär durch die Bindung von Substanz P (einem Peptid aus der Gruppe der Neurokinine) an Neurokinin-1‑Rezeptoren in der Area postrema im Brechzentrum. Ergänzend wird das antizipatorische Erbrechen definiert, das infolge einer negativen Konditionierung zu typischen Beschwerden führt.1 Aus dieser Pathophysiologie leitet sich die multimodale antiemetische Prophylaxe mit 5‑HT3‑Rezeptorantagonisten, NK1‑Rezeptorantagonisten und Dexamethason ab.
Risikofaktoren für CINV
Abgesehen von therapiebezogenen Risikofaktoren wie Behandlungsplan, Art, Dosis und Applikationsform der onkologischen Therapie spielen auch patientenindividuelle Risikofaktoren für CINV eine Rolle: Hierzu zählen weibliches Geschlecht, jüngeres Alter (< 50 Jahre), Ängstlichkeit, vorangegangene CINV und Reisekrankheit oder Schwangerschaftserbrechen in der Anamnese. Ein chronischer Alkoholabusus hingegen geht mit einem niedrigeren Risiko für diese Nebenwirkungen einher.2,3
Emetogenes Potential onkologischer Therapien
Die aktuelle MASCC/ESMO‑Klassifikation von 2023 teilt parenterale onkologische Therapien nach ihrem emetogenen Potential in vier Gruppen ein: minimal, gering, moderat oder hoch emetogen. Wirkstoffe mit hohem emetogenen Potenzial verursachen bei mehr als 90 % der Behandelten Übelkeit bzw. Erbrechen, moderat emetogene Wirkstoffe bei 30‒90 %, gering emetogene bei 10-30 % und minimal emetogene bei weniger als 10 %. Hoch emetogen sind beispielsweise Cisplatin, Dacarbazin, die Kombination aus Anthrazyklin und Cyclophosphamid (= AC-Schema) oder hochdosiertes Cyclophosphamid; moderat emetogen sind u. a. Carboplatin (am oberen Ende der moderaten Kategorie), Oxaliplatin und manche Antikörper‑Wirkstoff‑Konjugate (Trastuzumab deruxtecan und Sacituzumab govitecan). Taxane, Gemcitabin sowie zahlreiche monoklonale Antikörper und Checkpoint‑Inhibitoren zeigen hingegen ein geringes bis minimales emetogenes Risiko.2,3,4
Orale Tumortherapeutika – sogenannte Zytoralia ‒ werden entweder als minimal‑gering emetogen (Risiko bei < 30 % der Patient:innen) oder als moderat‑hoch emetogen (Risiko bei ≥ 30 % der Patient:innen) klassifiziert. Nachdem die Einnahme üblicherweise über einen längeren Zeitraum erfolgt, beschreibt das emetogene Risiko dabei den gesamten Einnahmezeitraum, nicht die ersten 24 Stunden nach der Einnahme (wie nach parenteraler Therapie). In die Kategorie moderat-hoch emetogen fallen u. a. Abemaciclib, Cabozantinib, Imatinib, Lenvatinib, Olaparib, Procarbazin, Ribociclib und Selinexor.4
Wirkstoffklassen von Antiemetika
5-HT3-Rezeptorantagonisten wie Ondansetron, Palonosetron und Granisetron unterdrücken durch Blockade von 5-HT3-Rezeptoren in Darm und Gehirn die Signalweiterleitung des Brechreflexes.
NK1-Rezeptor-Antagonisten wie Aprepitant, Fosaprepitant und Netupitant blockieren durch Bindung an den Neurokinin-1-Rezeptor im Gehirn die Wirkung von Substanz P und unterdrücken so den verzögerten Brechreiz.
Corticosteroide sind vor allem wirksam in der Prophylaxe von verzögerter Übelkeit und Erbrechen. Der
Wirkmechanismus ist nicht vollständig geklärt, wahrscheinlich spielen modulierende und antiphlogistische Eigenschaften eine Rolle. Sowohl Dexamethason als auch Prednison oder Prednisolon können eingesetzt werden, da jedoch in fast allen großen, randomisierten Studien Dexamethason als Corticosteroid verwendet wurde, gilt dieses als Standard.
Das atypische Neuroleptikum Olanzapin hat in den letzten Jahren in der antiemetischen Medikation zunehmend an Bedeutung gewonnen. Es blockiert neben Dopamin-D2-Rezeptoren weitere Signalwege, die in ihrer Gesamtheit die antiemetische Wirkung auslösen. Dieser Wirkstoff ist zur Antiemese nicht zugelassen, es handelt sich hierbei um einen Off-label-use.
Deutlich seltener werden andere Dopaminantagonisten wie Haloperidol oder Levomepromazin eingesetzt. Metoclopramid hat an Bedeutung verloren und wird (mit stark beschränkter Tageshöchstdosis) nur noch als Rescue-Medikament bei geringem emetogenem Risiko eingesetzt.
Zu den Reserveantiemetika gehören Benzodiazepine wie Lorazepam und Alprazolam, das H1-Antihistaminikum Dimenhydrinat und Cannabinoide.1,2
Empfohlene antiemetische Prophylaxe
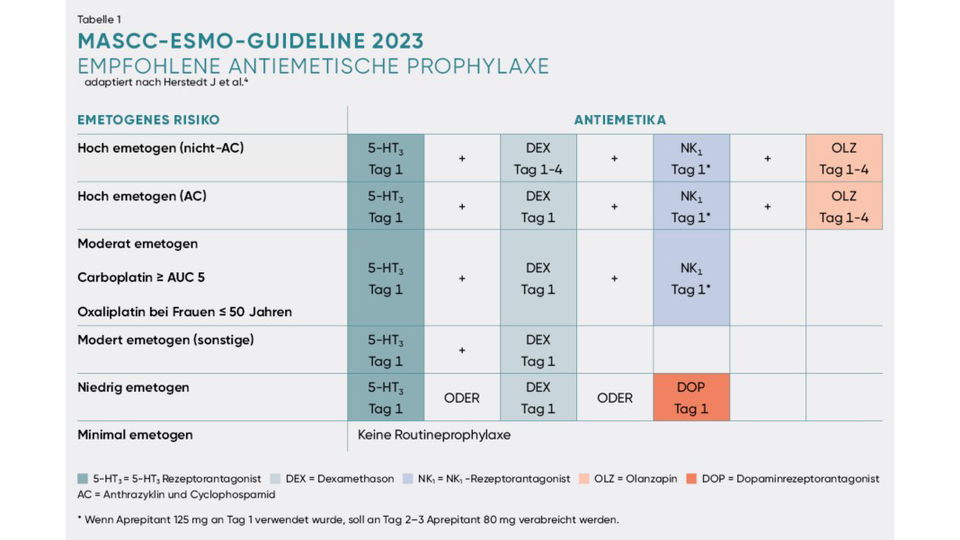
Durch eine optimale Prophylaxe können heutzutage selbst Patient:innen mit einer hoch emetogenen Tumortherapie zu 70 bis 80 % von Übelkeit und Erbrechen verschont bleiben. Die empfohlene antiemetische Prophylaxe richtet sich nach dem emetogenen Potenzial der onkologischen Therapie, bei Kombinationstherapien nach dem Wirkstoff mit dem größten emetogenen Potenzial. Bei hoch emetogenen Schemata kommt eine Vierfach-Prophylaxe (bestehend aus 5‑HT3‑RA, Dexamethason, NK1‑RA und Olanzapin) zum Einsatz, bei moderat emetogenen Therapien je nach Wirkstoff und Patientenrisiko eine Dreifach-Prophylaxe oder eine Zweierkombination, bei niedrig emetogenen Substanzen reicht eine Monotherapie, für minimal emetogene Wirkstoffe ist keine Routineprophylaxe empfohlen.4
Zur antiemetischen Prophylaxe bei Zytoralia-Therapie liegen weniger Daten vor, es gibt seitens der MASCC/ESMO keine generelle Empfehlung außer für eine Bedarfsmedikation. Die Onkopedia-Leitlinie „Antiemese bei medikamentöser Tumortherapie“ empfiehlt bei einer oralen Tumortherapie mit hohem/moderatem Risiko einen 5-HT3-RA an den Tagen eins bis sieben, kombiniert mit Dexamethason an den Tagen eins bis drei, anschließend soll die Antiemese abgesetzt und bei Bedarf als Rescue-Therapie erneut gestartet werden. Bei Procarbazin soll die Prophylaxe aufgrund des starken emetogenen Risikos mit einem NK1-RA ergänzt werden.3
Antizipatorische Nausea profitiert von verhaltenstherapeutischen Ansätzen, kurzzeitig niedrig dosierte Benzodiazepine können aufgrund ihrer anxiolytischen Eigenschaft in ausgewählten Fällen hilfreich sein.2,3
Radiotherapie‑ und Chemo‑Radiotherapie‑induzierte Übelkeit/Emesis (RINV/C‑RINV)
Auch bei einer Strahlentherapie kann es zu Übelkeit und Erbrechen kommen, insbesondere bei Ganzkörperbestrahlung sowie bei Bestrahlung des Bauchbereichs. Bei Radiatio mit hohem/moderatem Emetogenitätsrisiko sind 5‑HT3‑Antagonisten (+/- Dexamethason) Grundpfeiler der Prophylaxe. Patient:innen, die eine Strahlentherapie des Gehirns erhalten, sollten eine Rescuetherapie mit Dexamethason erhalten. Bei Radiatio an Kopf/Hals, Thorax oder Becken wird eine Bedarfstherapie mit Dexamethason, einem Dopamin-Rezeptorantagonisten oder einem 5-HT3-Rezeptorantagonisten empfohlen. Patient:innen unter Chemo-Radiotherapie sollten eine antiemetische Prophylaxe gemäß den antiemetischen Leitlinien der jeweils zutreffenden Chemotherapie-Risikokategorie erhalten – außer wenn das Risiko für Übelkeit und Erbrechen durch die Strahlentherapie höher ist als durch die Chemotherapie.5
Durchbruchs‑ und refraktäre Emesis
Treten trotz Prophylaxe Symptome auf, wird eine ergänzende Antiemese eingeleitet, die als Rescue-Therapie bezeichnet wird. Im darauffolgenden Behandlungszyklus wird die Prophylaxe dann individuell angepasst. Bei unzureichender Kontrolle von Übelkeit und Erbrechen trotz leitliniengerechter Prophylaxe sollten ein Wechsel der Wirkstoffklasse bzw. eine Therapieerweiterung (z. B. Olanzapin hinzufügen, 5‑HT3‑Rezeptorantagonist wechseln, Dopaminantagonisten für Rescue ergänzen) erwogen, Auslöser geprüft sowie Flüssigkeits- und Elektrolythaushalt gesichert werden. Wenn im Beratungsgespräch kein zeitlicher Zusammenhang von Übelkeit und Erbrechen mit der letzten Therapiesitzung hergestellt werden kann oder die Symptome heftiger als in vorherigen Behandlungszyklen sind, sollten mögliche Differenzialdiagnosen in Betracht gezogen werden – diese reichen von gastrointestinalen, zentralen oder hormonellen Ursachen über Stoffwechselstörungen bis hin zu möglichen Intoxikationen.2,3
Nebenwirkungsmanagement
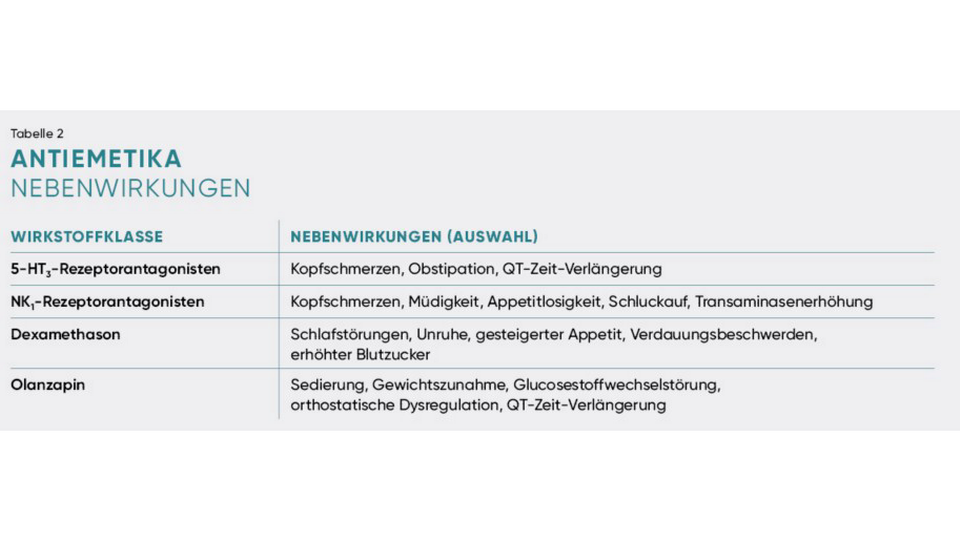
Eine Beratung durch den/die Apotheker:in zu den häufigsten Nebenwirkungen von Antiemetika und deren proaktivem Management kann die Adhärenz der Patient:innen fördern. Zum Beispiel empfiehlt sich bei älteren und vulnerablen Patient:innen zur Vermeidung der sedierenden Nebenwirkung von Olanzapin zu Therapiebeginn eine niedrige Anfangsdosis von 5 mg abends. Sollten Patient:innen besorgt sein, weil dieser Wirkstoff keine Zulassung zur Antiemese hat, kann auf die aktuellsten internationalen Therapieempfehlungen zum Einsatz von Olanzapin in dieser Indikation verwiesen werden. Diabetiker:innen sollten bei der Einnahme von Dexamethason besonders engmaschig ihren Blutzucker messen. Auch Wechselwirkungen spielen bei diesen Substanzklassen eine Rolle: Die CYP3A4-Hemmung durch Aprepitant ist Grund dafür, dass in der Kombination die Dosis von Dexamethason reduziert werden muss. Bei 5-HT3-RA besteht in Kombination mit anderen serotonergen Substanzen das Risiko für die Entstehung eines Serotoninsyndroms.2