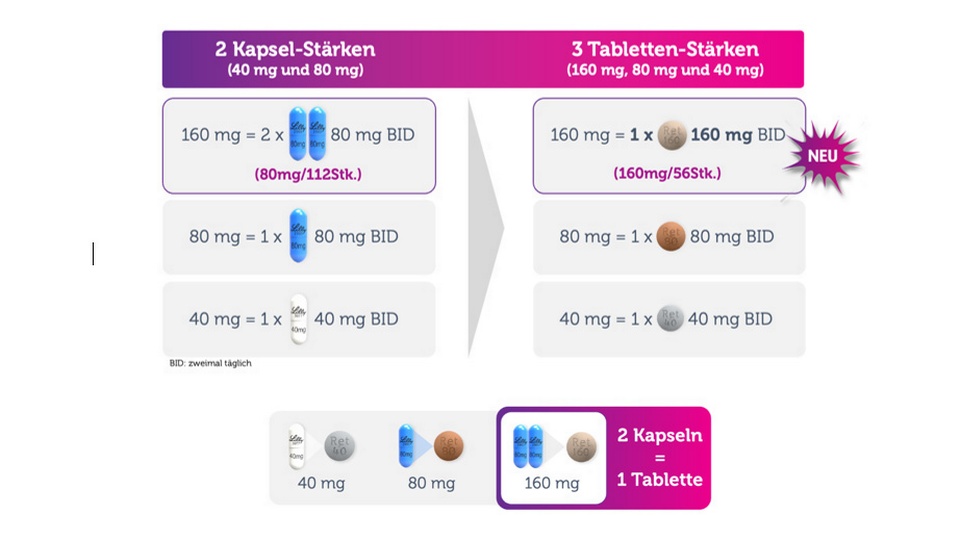
Warum kam es zu dieser Umstellung?
- Die Tabletten sind deutlich kleiner als die Kapseln.
- Die Tabletten sind einfacher zu schlucken.
- In der 160mg Dosis reduziert sich die Anzahl der Tabletten im Gegensatz zu den Kapseln.
- Bisher: 2x täglich 2 Kapseln zu 80mg (Monatspackung 80mg/112 Stück)
- NEU: 2 x täglich 1 Tablette zu 160mg (Monatspackung 160mg/56 Stück)
Einnahme:
Die Tabletten können entweder mit oder ohne Nahrung eingenommen werden. Die Tabletten sollen unzerkaut mit einem Glas Wasser geschluckt werden. Die Tabletten sollen vor dem Schlucken nicht gekaut, zerkleinert oder geteilt werden 2,3
Dosis:
Die empfohlene Dosierung von Selpercatinib hat sich nicht geändert! 1,2,3
Quellen
1. Fachinformation Retsevmo 40 [80] mg Hartkapseln. Aktueller Stand der Information 2.Fachinformation Retsevmo 40 [80, 160] mg Filmtabletten. Aktueller Stand der Information. 3.Gebrauchsinformation Retsevmo. Aktueller Stand der Information
FKI
Extramural wird Retsevmo® weiterhin exklusiv via Pharmacom Handels GmbH (https://b2b.pharma-com.at/de/Kontaktpublic) in Verkehr gebracht.
Dieses Arzneimittel unterliegt einer zusätzlichen Überwachung. Dies ermöglicht eine schnelle
Identifizierung neuer Erkenntnisse über die Sicherheit. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Hinweise zur Meldung von Nebenwirkungen, siehe Abschnitt 4.8 der Fachinformation.
1. BEZEICHNUNG DES ARZNEIMITTELS
Retsevmo ® 40 [80] mg Hartkapseln
Retsevmo ® 40 [80] [160] mg Filmtabletten
2. QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Jede Hartkapsel enthält 40 [80] mg Selpercatinib.
Jede Filmtablette enthält 40 [80] [160] mg Selpercatinib.
Vollständige Auflistung der sonstigen Bestandteile, siehe Abschnitt 6.1.
4.1 Anwendungsgebiete
Retsevmo als Monotherapie wird angewendet zur Behandlung von Erwachsenen mit:
– fortgeschrittenem RET-Fusions-positiven nicht-kleinzelligen Lungenkarzinom (NSCLC), die zuvor nicht mit einem RET-Inhibitor behandelt wurde – fortgeschrittenen RET-Fusions-positiven soliden Tumoren, wenn Behandlungsoptionen, die nicht auf RET abzielen, nur begrenzten klinischen Nutzen bieten oder ausgeschöpft sind (siehe Abschnitte 4.4 und 5.1) Retsevmo als Monotherapie wird angewendet zur Behandlung von Erwachsenen und Jugendlichen ab 12 Jahren
mit:
– fortgeschrittenem RET-Fusions-positiven Schilddrüsenkarzinom, das refraktär für radioaktives Iod ist
(wenn radioaktives Iod angemessen ist)
– fortgeschrittenem RET-mutierten medullären Schilddrüsenkarzinom (MTC)
4.3 Gegenanzeigen
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
6.1 Liste der sonstigen Bestandteile
Hartkapseln
Kapselinhalt: Mikrokristalline Cellulose, Hochdisperses Siliciumdioxid.
Kapselhülle: Retsevmo 40 mg Hartkapseln Gelatine, Titandioxid (E171), Eisen(Ⅱ, Ⅲ)-oxid; Retsevmo 80 mg Hartkapseln Gelatine, Titandioxid (E171), Brillantblau FCF (E133).
Kapseln: Zusammensetzung der schwarzen Farbe: Schellack, Ethanol 96 %, 2-Propanol (Ph. Eur.), Butan-1-ol, Propylenglycol, gereinigtes Wasser, konzentrierte Ammoniak-Lösung, Kaliumhydroxid
Eisen(Ⅱ, Ⅲ)-oxid.
Filmtabletten
Tablettenkern: Mikrokristalline Cellulose, Mannitol, Croscarmellose-Natrium, Hydroxypropylcellulose,
Natriumstearylfumarat.
Filmüberzug: Retsevmo 40 mg Filmtabletten: Poly(vinylalkohol), Titandioxid (E171), Macrogol, Talkum, Schwarzes Eisenoxid (E172); Retsevmo 80 mg Filmtabletten: Poly(vinylalkohol), Titandioxid (E171), Macrogol, Talkum, Rotes Eisenoxid (E172), Schwarzes Eisenoxid (E172); Retsevmo 160 mg Filmtabletten: Poly(vinylalkohol), Titandioxid (E171), Macrogol, Talkum, Rotes Eisenoxid (E172);
Pharmakotherapeutische Gruppe: Antineoplastische und immunmodulierende Mittel, antineoplastische
Mittel, Proteinkinase-Inhibitoren, ATC-Code: L01EX22
7. INHABER DER ZULASSUNG
Eli Lilly Nederland B.V., Papendorpseweg 83, 3528 BJ Utrecht, Niederlande
Abgabe: Rezept- und apothekenpflichtig, NR