Jahre darauf häuften sich Fälle von Herzrhythmusstörungen und sogar Todesfällen im Zusammenhang mit der Einnahme des Präparats, wodurch es letztendlich in den meisten Ländern vom Markt genommen wurde.
Terfenadin gilt als Paradebeispiel eines Medikaments, das eine signifikante Verlängerung der QT-Zeit bewirken kann und dadurch dosisabhängig kardio-toxisch wirkt. Arzneimittel sind häufig die Ursache für erworbene QT-Zeit-Verlängerungen, die im schlimmsten Fall zu lebensbedrohlichen Herzrhythmusstörungen führen können. Doch auch genetische Faktoren spielen eine Rolle: Beim angeborenen QT-Syndrom sind Mutationen in Genen, die für die Expression von kardialen Ionenkanälen kodieren, die Hauptursache.1-3
Was ist die QT-Zeit?
In einem Elektrokardiogramm (EKG) beschreibt die QT-Zeit das Intervall zwischen dem Start der Q-Welle und dem Ende der T-Welle. Sie dient als Marker für Depolarisation und Repolarisation von Myozyten und wird in Millisekunden (ms) angegeben (siehe Abbildung 1).
Messung und Messwerte der QT-Zeit
Die QT-Zeit ist von der Herzfrequenz abhängig und variiert deshalb mit zunehmender Aktivität. Bei körperlicher Belastung erhöht sich die Herzfrequenz, das RR-Intervall (1 s = 1.000 ms bei 60 Herzschlägen/min) wird kürzer und so auch das QT-Intervall. Deshalb muss mittels mathematischer Umrechnung das „korrigierte“ QTc-Intervall bestimmt werden, um einen von der Herzfrequenz unabhängigen Vergleichswert zu schaffen. Je nach Geschlecht und Alter kann die QTc-Zeit variieren. Bei Männern liegt sie im Normalfall unter 430 ms und bei Frauen unter 450 ms.
Das Aktionspotenzial der Herzmuskelzellen ist ein koordiniertes Zusammenspiel von verschiedenen Ionenkanälen an der Zellmembran mit depolarisierenden Einwärts- und repolarisierenden Auswärtsströmen. Bestimmte Arzneistoffe können an sogenannten hERG (human ether-a-go-go-related gene)-Kanälen, einer Gruppe von delayed rectifier K+-Kanälen (IKr), binden und diese blockieren. hERG-Kanäle sind wesentlich für die späte Repolarisation in der Phase 3 des Aktionspotenzials im Myokard. In der zentralen Pore des K+-Kanals finden sich spezifische Aminosäuren mit aromatischen und polaren Seitenketten, die als Bindungsstellen für Wirkstoffe fungieren.6
Durch die Blockade dieser Kaliumkanäle (IKr) verlängert sich die Repolarisationsdauer, was zu einer Verlängerung der QT-Zeit führt und im Myokard eine Heterogenität der Refraktärzeiten erzeugt. Spezielle Zellen in der mittleren Myokardschicht, sogenannte M-Zellen (Mid-myokardiale Zellen), sind besonders anfällig für diese Veränderungen, da sie physiologisch das längste Aktionspotenzial- und Repolarisationsintervall aufweisen. Diese Verlängerung erhöht die Wahrscheinlichkeit für frühe Nachdepolarisationen (EAD) in den M-Zellen. Diese EAD können ein Aktionspotenzial auslösen, das weitergeleitet wird und Extrasystolen verursacht. Die daraus resultierende nach außen gerichtete Erregungsfront der Extrasystole trifft aufgrund der unterschiedlichen Repolarisationszeiten im Myokard auf refraktäre und erregbare Zellen, was zu einer ungleichmäßigen Ausbreitung der Erregung führt. Dieser Mechanismus kann einen funktionellen Re-entry initiieren, der in eine Torsade-de Pointes (TdP)-Arrhythmie übergehen kann.5,7
Arzneimittel sind eine gängige Ursache für eine erworbene Verlängerung der QT-Zeit. Das Phänomen zählt zu den häufigsten Gründen für eine Marktrücknahme von Medikamenten.
Ähnlich wie bei Blutdruck und Blutzucker können diese Werte schwanken. Kurzzeitige Schwankungen um 40 ms nach oben oder unten können vorkommen. QTc-Zeiten bei Frauen über 470 ms und bei Männern über 450 ms gelten als verlängert. Bei QTc-Zeiten über 500 ms geht man von einem deutlich erhöhten Risiko für Torsade-de-Pointes (TdP)-Tachykardien aus.4
Wie wird die QTc-Zeit berechnet?
In der Literatur werden viele unterschiedliche Formeln genannt. Sehr häufig wird die Bazett-Formel für die Berechnung der QTc-Zeit verwendet, um die Frequenzkorrektur miteinzubeziehen:5

Ein Nachteil bei der Nutzung dieser Formel ist die Überkorrektur bei sehr hohen Herzfrequenzen. Bei Komedikation mit höheren Dosierungen von beispielsweise Anticholinergika und Sympathomimetika steigt die Herzfrequenz. Die Bazett-Formel wäre in diesem Zusammenhang ungeeignet.5 Ab einer Herzfrequenz von über 90 Schlägen/min wird daher die Friderica-Formel herangezogen:

Die genaueste – aber auch aufwendigste – Variante zur Auswertung wäre ein QT-Nomogramm, bei dem die gemessenen QT-Intervalle gegen die gemessenen Herzfrequenzen geplottet werden. Wenn die Werte der QT-Zeit bei der gemessenen Herzfrequenz über dem Cut-Off Wert liegen, spricht man von einer Verlängerung der QT-Zeit.2

Klinik
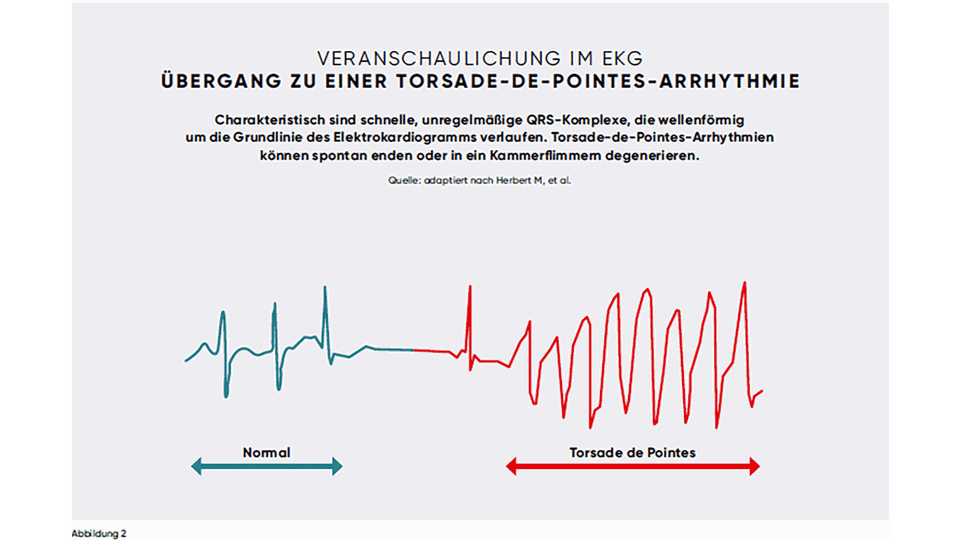
Symptome wie Palpitationen, Kollaps oder Synkopen sind ein klassisches Warnzeichen für ein Long-QT-Syndrom. Wird mittels EKG eine Torsade-de-Pointes-Arrhythmie festgestellt, gekennzeichnet durch einen wellenartigen Wechsel der Vektorachse des QRS-Komplexes (siehe Abbildung 2), muss sofort interveniert werden, da ein Übergang zu einem Kammerflimmern droht.

Körperlich können wiederholte Synkopen und Anfälle von Unwohlsein auftreten. Patient:innen mit dieser Sonderform der ventrikulären Tachykardie gehören intensivmedizinisch überwacht. Alle Medikamente, die als potenzieller Auslöser gelten, müssen sofort abgesetzt werden. Unabhängig vom Mg2+-Serumspiegel der Patient:innen wird im Regelfall Magnesiumsulfat intravenös verabreicht. Ebenso wird der Kaliumspiegel überwacht und gegebenenfalls auf Werte zwischen 4,5–5 mmol/l angehoben. Bradykardien stellen einen Risikofaktor dar, da sie eine Verlängerung der QT-Zeit verstärken. Deshalb wird in bestimmten Fällen intensivmedizinisch erwogen, die Herzfrequenz mittels Isoprenalin oder durch temporäres Pacing anzuheben.5–7
Das QT-Zeitverlängernde Potenzial eines Arzneistoffes ist dosisabhängig, daher spielen auch pharmakokinetische Wechselwirkungen eine Rolle.
• Weibliches Geschlecht
• Über 65 Jahre
• Gemeinsame Einnahme von mehreren
QT-Zeit-verlängernden Medikamenten
• Hypokaliämie
• Hypomagnesiämie
• Hypokalziämie
• Diuretikaeinnahme
• Bradykardie
• Kongenitales QT-Syndrom
• Herzinsuffizienz
• Digitalis-Therapie
• Hepatische und renale Einschränkungen
• Akuter Myokardinfarkt
• Sepsis
Medikamentös induziertes QT-Syndrom
Polypharmazie birgt in vielerlei Hinsicht ein Risiko für QT-Zeit-Verlängerungen. Pharmakodynamisch betrachtet steigt das Risiko für Rhythmusstörungen exponentiell, wenn zwei oder mehrere Medikamente eingenommen werden, die ein bekanntes Risiko für QT-Zeit-Verlängerung nachgewiesenermaßen erhöhen. Bekannte Beispiele dafür sind Neuroleptika wie Haloperidol oder Antidepressiva wie Imipramin. Mitunter haben auch mehrere Vertreter derselben Arzneistoffgruppe ein QT-Zeit-verlängerndes Potenzial, beispielsweise die Makrolid-Antibiotika Azithromycin und Clarithromycin oder die Fluorchinolone Levofloxacin, Moxifloxacin und Ciprofloxacin.5
Da das QT-Zeit-verlängernde Potenzial eines Arzneistoffes dosisabhängig ist, spielen auch pharmakokinetische Wechselwirkungen eine Rolle. Eine ganze Reihe weiterer (klinischer) Faktoren haben einen Einfluss auf eine Verlängerung der QT-Zeit (siehe Kasten 2). Besonders hervorzuheben nach einem heißen Sommer sind Elektrolytentgleisungen, sei es durch vermehrtes Schwitzen, Erbrechen oder Durchfall. Speziell Hypokaliämie, Hypokalziämie und Hypomagnesiämie sind Risikofaktoren für eine Verlängerung der QT-Zeit. Auch Arzneistoffe wie z. B. Schleifendiuretika, die eine Elektrolytentgleisung verstärken können, stellen ein Problem dar.5,7
Spezielle Tools wie der Tisdale Risk Score helfen, das Risiko von QT-Zeit-Verlängerungen und deren Komplikationen abzuschätzen.5 Das Arizona Center for Education and Research on Therapeutics (AZCERT) bietet mit www.crediblemeds.org eine aktualisierte Datenbank, die eine Einschätzung zum QT-verlängernden Potenzial und dem Risiko für Torsade-de-Pointes-Arrhythmien aufzeigt.8,9
Angeborenes Long-QT-Syndrom
Etwa 10 % der Betroffenen eines angeborenen Long-QT-Syndroms (LQTS) zeigen in den ersten drei Lebensjahren erste Anzeichen. Typische kardiale Symptome sind Schwindel, Synkopen und Herzrasen, die je nach genetischer Unterform durch unterschiedliche Trigger ausgelöst werden können. Ein besonders häufiger Auslöser, insbesondere beim Long-QT-Syndrom Typ 1 (LQT1), ist der akute Kontakt mit Wasser. Besonders bei Kindern und Jugendlichen lässt sich ein erhöhtes Risiko für tödliche kardiale Ereignisse im Zusammenhang mit Wasserkontakt feststellen. Genetische Autopsien haben gezeigt, dass über 10 % der ungeklärten Todesfälle bei Kindern und Jugendlichen, die beim Schwimmen oder Tauchen auftreten, auf das Vorliegen eines Long-QT-Syndroms zurückzuführen sind.4

Für das Long-QT-Syndrom sind bislang 13 verschiedene Gene (LQT1 bis LQT13) auf fünf unterschiedlichen Chromosomen mit mehr als 600 bekannten Mutationen identifiziert. Die Prävalenz in der Allgemeinbevölkerung liegt bei etwa 1:2.500 und ist damit häufiger, als früher angenommen wurde. Verschiedene Mutationen in Genen, die Ionenkanäle kodieren, verursachen die angeborene Form des Syndroms. Die drei häufigsten genetischen Subtypen sind LQT1, LQT2 und LQT3, die zusammen etwa 75 % aller Fälle ausmachen.4,6
• LQT-1: Diese häufigste Form (40–55 % der Fälle) wird durch eine Mutation für den spannungsabhängigen Kaliumkanal KVLQT1 (oder KCNQ1) verursacht. Betroffene haben oft Probleme bei körperlicher Belastung und sportlichen Aktivitäten, insbesondere beim Schwimmen und Tauchen.4,6
• LQT-2: Diese Form ist durch eine Mutation im Gen, das für den hERG-Kanal auf Chromosom 7 kodiert, bedingt. Mutationen, die die Porenregion des Kanals betreffen, erhöhen das Risiko für kardiale Ereignisse. Mutationen außerhalb der Porenregion sind häufig mit einem höheren Risiko für TdP-Arrhythmien, besonders bei Hypokaliämie, verbunden. Emotionale Belastungen oder Schrecksituationen wie das Läuten eines Weckers sind bekannte Trigger.4,6
• LQT-3: Diese Form betrifft Mutationen im Natriumkanal SCN5A. Symptome treten häufiger in Ruhephasen bei niedrigem Puls oder während des Tiefschlafs auf.4
Die Behandlung des Long-QT-Syndroms umfasst drei wichtige Komponenten: medikamentöse Therapie, elektrische Kardioversion im Notfall und Anpassung des Lebensstils sowie Vermeidung von Triggern. Betablocker wie Propranolol werden am häufigsten eingesetzt, um die Wahrscheinlichkeit tödlicher kardialer Ereignisse von 70 % auf 10 % zu reduzieren. Diese Behandlung zeigt die beste Wirksamkeit bei LQT-1 und die geringste bei LQT-3. Bei LQT-3 wird oft eine Kombination aus Betablockern und Mexiletin verwendet, da hier auf molekularer Ebene betrachtet ein anderer Ionenkanal betroffen ist.4
Folgende Kernpunkte sind zu beachten:
• Neu verordnete Medikamente sollten auf ihr Risiko überprüft werden.
• Nutzen-Risiko-Abschätzung bei Neuverordnung eines QT-Zeit-verlängernden Medikaments
• Auch pharmakokinetische Wechselwirkung im Auge behalten (z. B. durch CYP-Inhibitoren)
• Vor allem bei Risikogruppen sollte vor und nach der Aufdosierungsphase eines QT-Zeit- verlängernden Medikaments (z. B. Neuroleptikum) ein EKG geschrieben werden.
• Patientenaufklärung über Symptome wie
Palpitationen, Kollaps oder Synkopen
• Regelmäßige Elektrolytkontrollen speziell
von K+, Mg2+, Ca2+ von Vorteil (speziell bei Diuretikaeinnahme)
Quellen
1. arznei-telegramm. Marktverbote und Verschreibungspflicht für Antiallergikum Terfenadin (TELDANE u.a.). arznei-telegramm (1997).
2. Isbister GK. Risk Assessment of Drug-Induced QT Prolongation. www.australianprescriber.com.
3. Vandael, E., Vandenberk, B., Vandenberghe, J., Willems, R. & Foulon, V. Risk factors for QTc-prolongation: systematic review of the evidence. Int J Clin Pharm 39, 16–25 (2017).
4. Herbert, M., Ulmer, E. & Na, N. +. Das Long-QT-Syndrom (LQTS): Über den lebenslangen Umgang mit einer genetisch bedingten Herzerkrankung.
5. Duckheim M., et al.:. Polypharmazie – Medikamente und QTc-Zeit. Was ist zu beachten? doi:10.1055/a-1166-2647.
Weitere Literatur auf Anfrage